Fraccionamiento y centrifugación
De Wikillerato
| (Una edición intermedia no se muestra.) | |||
| Línea 3: | Línea 3: | ||
La ultracentriguga es un instrumento habitual de los laboratorios de Bioquímica y Biología molecular, fue inventada por el químico sueco Theodor Svedberg (1884-1971) en 1925 (recibió el premio Nobel en 1926 por este desarrollo instrumental y por sus estudios en la química de los coloides), puede proporcionar campos centrífugos que superan 250.000 veces la fuerza de la gravedad. Un campo centrífugo tan elevado provoca la sedimentación de las partículas (e.g. proteínas, ribosomas) al oponerse esa fuerza centrífuga a la fuerza de difusión la cual tiende normalmente a mantenerlas uniformente dispersas en la disolución. En el método llamado de''' velocidad de sedimentación''', se somete a ultracentrifugación en un tubo a una disolución generalmente acuosa de las partículas hasta que se alcanza una velocidad constante de sedimentación de las mismas, cuando el frente de sedimentación (formado cuando la fuerza centrífuga supera la fuerza de difusión) de la partículas se mueve a velocidad constante, la fuerza centrífuga contrarresta exactamente la resistencia a la fricción del disolvente, debido a que la fuerza centrifuga aplicada por la ultracentrífuca (de varios cientos de miles de ''g'') es cancelada por la resistencia viscosa del medio (normalmente agua) a través del cual la partícula se mueve dentro del tubo | La ultracentriguga es un instrumento habitual de los laboratorios de Bioquímica y Biología molecular, fue inventada por el químico sueco Theodor Svedberg (1884-1971) en 1925 (recibió el premio Nobel en 1926 por este desarrollo instrumental y por sus estudios en la química de los coloides), puede proporcionar campos centrífugos que superan 250.000 veces la fuerza de la gravedad. Un campo centrífugo tan elevado provoca la sedimentación de las partículas (e.g. proteínas, ribosomas) al oponerse esa fuerza centrífuga a la fuerza de difusión la cual tiende normalmente a mantenerlas uniformente dispersas en la disolución. En el método llamado de''' velocidad de sedimentación''', se somete a ultracentrifugación en un tubo a una disolución generalmente acuosa de las partículas hasta que se alcanza una velocidad constante de sedimentación de las mismas, cuando el frente de sedimentación (formado cuando la fuerza centrífuga supera la fuerza de difusión) de la partículas se mueve a velocidad constante, la fuerza centrífuga contrarresta exactamente la resistencia a la fricción del disolvente, debido a que la fuerza centrifuga aplicada por la ultracentrífuca (de varios cientos de miles de ''g'') es cancelada por la resistencia viscosa del medio (normalmente agua) a través del cual la partícula se mueve dentro del tubo | ||
| - | El '''coeficiente de sedimentación''' de una partícula o macromolécula se calcula dividiendo la velocidad (constante) de sedimentación (<math>dx/dt</math>, en m/s) por la aceleración aplicada en m/s^2 (<math>{w^2x}</math>, donde <math>w</math>, es la velocidad angular [[http://portales.educared.net/wikiEducared/index.php?title=Movimiento_circular_uniforme]] del giro del rotor de la ultracentrífuca y <math>x</math> la distancia desde el centro de rotación), matemáticamente <math> s = \frac{dx/dt}{w^2x}</math> , por lo tanto el coeficiente de sedimentación tiene las dimensión de unidades de tiempo y expresado en Svedbergs. Un Svedberg es definido exactamente como 1x 10^−13 segundos (s). Por ejemplo el coeficiente de sedimentación de 8x 10^−13 s, se representa por '''8S'''. Así por ejemplo, las subunidades de los ribosomas procariotas tienen coeficientes de sedimentación de 30S para la subunidad menor y 50S para la subunidad mayor [[http://portales.educared.net/wikiEducared/index.php?title=Ribosomas]] . Los coeficientes de sedimentación no son aditivos, pues aunque el coeficiente de sedimentación aumenta con el peso molecular, no es proporcional al mismo, ya que está influido también por la resistencia a la fricción del disolvente y por la forma tridimensional (3D) de la partícula. Así por ejemplo, el ribosoma procariota completo constituido por una subunidad mayor unida a una menor tiene un coeficiente de sedimentación 70S que por lo tanto no es igual a la suma de los coeficientes 30S + 50S obtenidos para las subunidades ribosómicas por separado. | + | El '''coeficiente de sedimentación''' de una partícula o macromolécula se calcula dividiendo la velocidad (constante) de sedimentación (<math>dx/dt</math>, en m/s) por la aceleración aplicada en m/s^2 (<math>{w^2x}</math>, donde <math>w</math>, es la velocidad angular [[http://portales.educared.net/wikiEducared/index.php?title=Movimiento_circular_uniforme]] ,expresada en radianes por segundo, del giro del rotor de la ultracentrífuca y <math>x</math> la distancia desde el centro de rotación), matemáticamente <math> s = \frac{dx/dt}{w^2x}</math> , por lo tanto el coeficiente de sedimentación tiene las dimensión de unidades de tiempo y expresado en Svedbergs. Un Svedberg es definido exactamente como 1x 10^−13 segundos (s). Por ejemplo el coeficiente de sedimentación de 8x 10^−13 s, se representa por '''8S'''. Así por ejemplo, las subunidades de los ribosomas procariotas tienen coeficientes de sedimentación de 30S para la subunidad menor y 50S para la subunidad mayor [[http://portales.educared.net/wikiEducared/index.php?title=Ribosomas]] . Los coeficientes de sedimentación no son aditivos, pues aunque el coeficiente de sedimentación aumenta con el peso molecular, no es proporcional al mismo, ya que está influido también por la resistencia a la fricción del disolvente y por la forma tridimensional (3D) de la partícula. Así por ejemplo, el ribosoma procariota completo constituido por una subunidad mayor 50S unida a una menor 30S tiene un coeficiente de sedimentación 70S que por lo tanto no es igual a la suma de los coeficientes 30S + 50S obtenidos para las subunidades ribosómicas por separado. |
[[Categoría: Biología]] | [[Categoría: Biología]] | ||
Revisión actual
Ultracentrifugación y el coeficiente Svedberg de sedimentación
La ultracentriguga es un instrumento habitual de los laboratorios de Bioquímica y Biología molecular, fue inventada por el químico sueco Theodor Svedberg (1884-1971) en 1925 (recibió el premio Nobel en 1926 por este desarrollo instrumental y por sus estudios en la química de los coloides), puede proporcionar campos centrífugos que superan 250.000 veces la fuerza de la gravedad. Un campo centrífugo tan elevado provoca la sedimentación de las partículas (e.g. proteínas, ribosomas) al oponerse esa fuerza centrífuga a la fuerza de difusión la cual tiende normalmente a mantenerlas uniformente dispersas en la disolución. En el método llamado de velocidad de sedimentación, se somete a ultracentrifugación en un tubo a una disolución generalmente acuosa de las partículas hasta que se alcanza una velocidad constante de sedimentación de las mismas, cuando el frente de sedimentación (formado cuando la fuerza centrífuga supera la fuerza de difusión) de la partículas se mueve a velocidad constante, la fuerza centrífuga contrarresta exactamente la resistencia a la fricción del disolvente, debido a que la fuerza centrifuga aplicada por la ultracentrífuca (de varios cientos de miles de g) es cancelada por la resistencia viscosa del medio (normalmente agua) a través del cual la partícula se mueve dentro del tubo
El coeficiente de sedimentación de una partícula o macromolécula se calcula dividiendo la velocidad (constante) de sedimentación (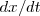 , en m/s) por la aceleración aplicada en m/s^2 (
, en m/s) por la aceleración aplicada en m/s^2 (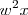 , donde
, donde 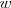 , es la velocidad angular [[1]] ,expresada en radianes por segundo, del giro del rotor de la ultracentrífuca y
, es la velocidad angular [[1]] ,expresada en radianes por segundo, del giro del rotor de la ultracentrífuca y  la distancia desde el centro de rotación), matemáticamente
la distancia desde el centro de rotación), matemáticamente 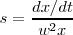 , por lo tanto el coeficiente de sedimentación tiene las dimensión de unidades de tiempo y expresado en Svedbergs. Un Svedberg es definido exactamente como 1x 10^−13 segundos (s). Por ejemplo el coeficiente de sedimentación de 8x 10^−13 s, se representa por 8S. Así por ejemplo, las subunidades de los ribosomas procariotas tienen coeficientes de sedimentación de 30S para la subunidad menor y 50S para la subunidad mayor [[2]] . Los coeficientes de sedimentación no son aditivos, pues aunque el coeficiente de sedimentación aumenta con el peso molecular, no es proporcional al mismo, ya que está influido también por la resistencia a la fricción del disolvente y por la forma tridimensional (3D) de la partícula. Así por ejemplo, el ribosoma procariota completo constituido por una subunidad mayor 50S unida a una menor 30S tiene un coeficiente de sedimentación 70S que por lo tanto no es igual a la suma de los coeficientes 30S + 50S obtenidos para las subunidades ribosómicas por separado.
, por lo tanto el coeficiente de sedimentación tiene las dimensión de unidades de tiempo y expresado en Svedbergs. Un Svedberg es definido exactamente como 1x 10^−13 segundos (s). Por ejemplo el coeficiente de sedimentación de 8x 10^−13 s, se representa por 8S. Así por ejemplo, las subunidades de los ribosomas procariotas tienen coeficientes de sedimentación de 30S para la subunidad menor y 50S para la subunidad mayor [[2]] . Los coeficientes de sedimentación no son aditivos, pues aunque el coeficiente de sedimentación aumenta con el peso molecular, no es proporcional al mismo, ya que está influido también por la resistencia a la fricción del disolvente y por la forma tridimensional (3D) de la partícula. Así por ejemplo, el ribosoma procariota completo constituido por una subunidad mayor 50S unida a una menor 30S tiene un coeficiente de sedimentación 70S que por lo tanto no es igual a la suma de los coeficientes 30S + 50S obtenidos para las subunidades ribosómicas por separado.



