Postulados de Bohr
De Wikillerato
Chemaseg (Discutir | contribuciones)
(Página nueva: El físico danes Niels H.D. Borh (1885-1962) propuso un modelo en 1913 publicado en la revista ''Philosophical Magazine'' para el átomo de hidrógeno en el que combinaba el trabajo...)
Ir a las siguientes diferencias →
Revisión de 18:33 25 nov 2008
El físico danes Niels H.D. Borh (1885-1962) propuso un modelo en 1913 publicado en la revista Philosophical Magazine para el átomo de hidrógeno en el que combinaba el trabajo de Planck, Einstein y Rutherford y que tubo un éxito muy destacado en predecir el ciertas características del espectro de hidrógeno observadas experimentalmente.
Antecedentes históricos a la propuesta de Bohr
El modelo atómico planetario propuesto en 1911 por el físico neozelandés Ernest Rutherford (1871-1937) en base a los experimentos de borbamdeando de finas láminas de átomos de oro con partículas 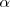 (núcleos de átomos de helio) que los científicos alemanes Hans W. Geiger (1882-1945) y sir Ernest Marsden (1889-1970) habían realizaron en bajo su dirección (entonces eran sus alumnos), suponía la existencia en el átomo de un núcleo de pequeño tamaño (~[Unparseable or potentially dangerous latex formula. Error 3 ]) y volumen en relación con el resto del átomo completo ([Unparseable or potentially dangerous latex formula. Error 3 ]) donde se concentra la mayoría de la masa atómica, estando cargado positivamente y con los electrones de carga negativa orbitando (girando) alrededor del mismo unidos por la atracción electrostática del núcleo, al igual que los planetas que orbitan alrededor del Sol.
(núcleos de átomos de helio) que los científicos alemanes Hans W. Geiger (1882-1945) y sir Ernest Marsden (1889-1970) habían realizaron en bajo su dirección (entonces eran sus alumnos), suponía la existencia en el átomo de un núcleo de pequeño tamaño (~[Unparseable or potentially dangerous latex formula. Error 3 ]) y volumen en relación con el resto del átomo completo ([Unparseable or potentially dangerous latex formula. Error 3 ]) donde se concentra la mayoría de la masa atómica, estando cargado positivamente y con los electrones de carga negativa orbitando (girando) alrededor del mismo unidos por la atracción electrostática del núcleo, al igual que los planetas que orbitan alrededor del Sol.
La mecánica clásica permitía un modelo de órbitas circulares y elípticas para el electrón en este modelo planetario. Por ejemplo, el átomo más sencillo de todos, el átomo de hidrógeno, constaría de un electrón y un núcleo positivo (con un protón) la carga del núcleo es la misma que la del electrón pero de signo contrario, por lo que el átomo es eléctricamente neutro. Este modelo planetario es estable mecánicamente, debido a que el potencial de Coulomb:
[Unparseable or potentially dangerous latex formula. Error 3 ] ![[1] [1]](/images/math/math-7edb124f6e6e3c0bd88bf6282a8e603a.png)
proporciona la fuerza centrípeta:
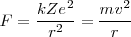
![[2] [2]](/images/math/math-ec736101c15bd1d1133c7e3d7015ddd9.png)
necesaria para que el electrón se mueva en un circulo de radio  a una velocidad
a una velocidad  . Pero es eléctricamente inestable debido a que el electrón está siempre acelerando hacia el centro del círculo. Las leyes de la electrodinámica clásica (ley de Larmor) predicen que una carga acelerando radia luz con una frecuencia igual al periodo del movimiento, en este caso la frecuencia de revolución
. Pero es eléctricamente inestable debido a que el electrón está siempre acelerando hacia el centro del círculo. Las leyes de la electrodinámica clásica (ley de Larmor) predicen que una carga acelerando radia luz con una frecuencia igual al periodo del movimiento, en este caso la frecuencia de revolución  .
.
Así clasicamente tenemos que:
[Unparseable or potentially dangerous latex formula. Error 3 ]=[Unparseable or potentially dangerous latex formula. Error 3 ]~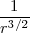
![[3] [3]](/images/math/math-5997f14afe377dff877df1d1629d9c02.png)
La energía total del electrón es la suma de ls energías cinética y potencial:
[Unparseable or potentially dangerous latex formula. Error 3 ] ![[4] [4]](/images/math/math-b89757a59b41b6506218bd6647cd5ee7.png)
A partir de la ecuación ![[1] [1]](/images/math/math-7edb124f6e6e3c0bd88bf6282a8e603a.png) se tiene que
se tiene que 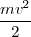 =
=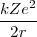 (un resultado que se mantiene para el movimiento circular [[1]] en un campo de fuerza central que varía con el inverso de la distancia al cuadrado), así que la energía total puede ser descrita como:
(un resultado que se mantiene para el movimiento circular [[1]] en un campo de fuerza central que varía con el inverso de la distancia al cuadrado), así que la energía total puede ser descrita como:
[Unparseable or potentially dangerous latex formula. Error 3 ]= [Unparseable or potentially dangerous latex formula. Error 3 ] ~ 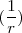
![[5] [5]](/images/math/math-311713d7e899562efc3b7c08c8a01ccb.png)
Así la física clásica predice que debido a que la energía es perdida por radiación el tamaño de la órbita del electrón alrededor del núcleo (dado por  ) se irá reduciendo cada vez más haciéndose cada vez más pequeña, incrementándose de igual manera la tasa en la cual la energía del electrón es perdida, el proceso que terminaría cuando el electrón alcanzara el núcleo, colapsando con el mismo. Este tiempo puede ser calculado por la mecánica y electrodinámica clásica y resultaría ser menos de un microsegundo. Así, el modelo planetario clásico para el átomo predice que este debería radiar un espectro continuo (ya que la frecuencia de revolución cambia continuamente cuando el electrón cae en espiral hacia el núcleo) y que se produciría un colapso cuando el electrón se precipitara contra el núcleo, un resultado que afortunadamente no ocurre. Es decir según este modelo el átomo es una entidad inestable, llamada a desaparecer con el tiempo. Experimentalmente se comprueba todo lo contrario que a no ser que el átomo sea excitado, el átomo no radia, no emite radiación electromagnética y que cuando es excitado el átomo radia una línea espectral discreta y no un espectro de radiación continua.
) se irá reduciendo cada vez más haciéndose cada vez más pequeña, incrementándose de igual manera la tasa en la cual la energía del electrón es perdida, el proceso que terminaría cuando el electrón alcanzara el núcleo, colapsando con el mismo. Este tiempo puede ser calculado por la mecánica y electrodinámica clásica y resultaría ser menos de un microsegundo. Así, el modelo planetario clásico para el átomo predice que este debería radiar un espectro continuo (ya que la frecuencia de revolución cambia continuamente cuando el electrón cae en espiral hacia el núcleo) y que se produciría un colapso cuando el electrón se precipitara contra el núcleo, un resultado que afortunadamente no ocurre. Es decir según este modelo el átomo es una entidad inestable, llamada a desaparecer con el tiempo. Experimentalmente se comprueba todo lo contrario que a no ser que el átomo sea excitado, el átomo no radia, no emite radiación electromagnética y que cuando es excitado el átomo radia una línea espectral discreta y no un espectro de radiación continua.
Para “solucionar” estas dificultades inabordables desde un punto de vista clásico, Bohr introdujo ad hoc en su modelo de 1913 una serie de postulados no clásicos de naturaleza cuántica, introduciendo con ello la cuantificación (cuantización) iniciada por Planck y Einstein en el “corazón” de la estructura del átomo.
Postulados del modelo atómico de Bohr
Primer postulado:
Los electrones se mueven en ciertas órbitas permitidas alrededor del núcleo sin emitir radiación. Así Bohr asumió que el átomo de hidrógeno puede existir solo en ciertos estados discretos, los cuales son denominados estados estacionarios del átomo. En el átomo no hay emisión de radiación electromagnética mientras el electrón no cambia de órbita.
Con este postulado Bohr evitaba el problema de la inestabiliad orbital eléctrica del electrón que predice la electrodinámica clásica y por tanto del átomo, al postular que la radiación de energía por parte de las partículas cargadas es válida a escala macroscópica pero no es aplicable al mundo microscópico del átomo, pero si esto es así surge el problema de de explicar la transición entre los estados estacionarios y la emisión de radiación por el átomo para ello Borh introdujo otro postulado :
Segundo postulado:
El átomo radia cuando el electrón hace una transición (“salto”) desde un estado estacionario a otro, es decir toda emisión o absorción de radiación entre un sistema atómico esta generada por la transición entre dos estados estacionarios. La radiación emitida (o absorbida) durante la transición corresponde a un cuanto de energía (fotón) cuya frecuencia  esta relacionada con las energías de las órbitas estacionarias por la ecuación de Planck:
esta relacionada con las energías de las órbitas estacionarias por la ecuación de Planck: 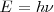
y está determinada por la relación :
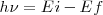
![[3] [3]](/images/math/math-5997f14afe377dff877df1d1629d9c02.png)
donde 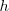 es la constante de Planck, con
es la constante de Planck, con 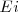 y
y 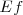 son las energías de los estados estacionarios iniciales y finales de la transición electrónica. La ecuación
son las energías de los estados estacionarios iniciales y finales de la transición electrónica. La ecuación ![[3] [3]](/images/math/math-5997f14afe377dff877df1d1629d9c02.png) es referida como la condición de frecuencia de Bohr.
es referida como la condición de frecuencia de Bohr.
Este postulado está basado en el concepto de fotón introducido por Einstein [[2]], junto con la conservación de la energía; si la luz está compuesta de fotones de energía , la emisión por parte del átomo de un fotón debe suponer una pérdida de energía igual a la energía del fotón emitido (o si es la absorción de un fotón a la ganancia de energía), por lo tanto es un postulado equivalente aquel de la conservación de la energía con la emisión del fotón, es crucial, debido a que con el Bohr se desvía “de la senda de la teoría clásica”, que requiere que la frecuencia de radiación sea igual a la frecuencia del movimiento de la partícula cargada. Así, mientras el equilibrio dinámico mecánico del sistema en los estados estacionarios está regido por las leyes ordinarias de la mecánica, sin embargo, dichas leyes no son aplicables cuando se trata de transiciones entre estados estacionarios.
Tercer postulado:
Las órbitas estacionarias admisibles son aquellas en las que el momento angular orbital 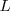 del electrón está cuantizado, pudiendo este asumir solamente valores múltiplos enteros de
del electrón está cuantizado, pudiendo este asumir solamente valores múltiplos enteros de 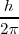 , donde
, donde  es un número integral (
es un número integral (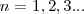 ), llamado numero cuántico principal. Así,
), llamado numero cuántico principal. Así,
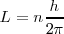
Este postulado Bohr introduce de nuevo la idea de cuantización en una nueva área de la física clásica al presuponer la idea de cuantización del momento angular orbital de un electrón que se mueve bajo la acción de una fuerza culombinana.



