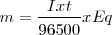Las cubas electrolíticas. Constante de Faraday
De Wikillerato
Electrólisis
Mientras que las pilas o células galvánicas son dispositivos que producen energía eléctrica al consumir energía química, la electrolisis representa el fenómeno opuesto. En este la energía eléctrica es consumida para realizar un proceso químico no espontáneo. Así se puede formular la siguiente definición:
Se llama electrolisis al proceso redox no espontáneo que tiene lugar al paso de una corriente eléctrica continua a través de una electrólito, disuelto o fundido
O en forma más resumida:
Se llama electrolisis al proceso que utiliza una corriente eléctrica para producir un cambio químico
Electrólisis del cloruro de sodio fundido
El 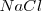 fundido se electroliza en una cuba o célula electrolítica. La cuba tiene dos electrodos que se sumergen en un electrolito y que están conectados a una batería. A través de los dos electrodos se hace pasar la corriente eléctrica. Los electrones llegan al líquido a través del electrodo negativo, el cátodo, que atrae a los cationes
fundido se electroliza en una cuba o célula electrolítica. La cuba tiene dos electrodos que se sumergen en un electrolito y que están conectados a una batería. A través de los dos electrodos se hace pasar la corriente eléctrica. Los electrones llegan al líquido a través del electrodo negativo, el cátodo, que atrae a los cationes 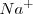 , los cuales al combinarse con dichos electrones suministrados por la batería, siendo reducidos a metal de sólido donde se deposita el sodio metálico, y salen por el electrodo positivo, el ánodo, el electrodo positivo (ánodo) atrae a los aniones
, los cuales al combinarse con dichos electrones suministrados por la batería, siendo reducidos a metal de sólido donde se deposita el sodio metálico, y salen por el electrodo positivo, el ánodo, el electrodo positivo (ánodo) atrae a los aniones 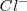 , que reponen los electrones quitados por la batería y por lo tanto oxidando al cloro, donde se observa producción de burbujas de cloro gaseoso:
, que reponen los electrones quitados por la batería y por lo tanto oxidando al cloro, donde se observa producción de burbujas de cloro gaseoso:
Las reacciones en los electrodos y la reacción global son:
Reacción catódica (reducción): 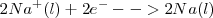
Reacción anódica (oxidación): 
Reacción global: 
En esta reacción pues el sodio ha actuado como oxidante frente al cloro. Esta reacción no es espontánea, así este fenómeno no espontáneo ha sido posible mediante la aplicación de una energía proporcionada por el generador eléctrico externo conectado a la cuba.
Así como en las células o pilas galvánicas, el ánodo es el electrodo donde la reacción de oxidación tiene lugar y el cátodo es el electrodo donde la reacción tiene lugar. Sin embargo, el signo de los electrodos es opuesto en las dos clases de células. En una pila galvánica es ánodo es considerado el negativo debido a que proporciona electrones al circuito externo, pero en una cuba electrolítica, el ánodo es considerado positivo porque los electrones son empujados hacia fuera de él por la batería.
Leyes de Faraday
La ciencia necesita realizar una cuantificación lo más precisa de lo que ocurre en los fenómenos naturales. El gran físico inglés Michael Faraday (1791-1867) inicio en 1830 el estudio cuantitativo de la relación que existía entre la cantidad de electricidad que atraviesa una disolución y la cantidad de sustancia transformada.
Faraday fue uno de los pioneros que asentaron la base de la electroquímica, acuñando los términos fundamentales de la misma: electrolito, para la disolución que conduce la corriente eléctrica; electrodos, para las piezas metálicas por las que entra o sale la corriente eléctrica en contacto con la disolución; ánodo, el conectado al polo positivo del generador, y cátodo el conectado al polo negativo; iones (que en griego significa “viajero”) las partículas que forman la corriente eléctrica en el seno de la disolución, nombrando como cationes a los que viajan hacia el cátodo, y aniones a los que se dirigen hacia el ánodo.
Sus experiencias fueron resumidas en las conocidas como Leyes de Faraday de la electrólisis:
1ª Ley, la cantidad de un elemento que se produce en un electrodo es directamente proporcional a la cantidad de electricidad (carga eléctrica) que atraviesa dicho electrodo
2ª Ley, para una misma cantidad de electricidad, lo pesos de distintos elementos liberados en el electrodo son directamente proporcionales a sus equivalentes químicos (“equivalentes redox”).
En relación a la primera ley, la carga eléctrica transportada (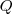 ) por una corriente continua es directamente proporcionar al tiempo (
) por una corriente continua es directamente proporcionar al tiempo (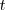 ): cuantitativamente
): cuantitativamente 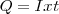 , siendo
, siendo 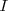 la intensidad de corriente eléctrica. Si se hace pasar por una cuba electrolítica cierta intensidad durante diferentes lapsos de tiempo, las masas de un mismo elemento se muestran proporcionales a las respectivas cargas que han pasado por los electrodos. Por otra parte si se ponen en varias cubas en serie con distintos electrodos y disoluciones, es claro que la carga eléctrica que pasa es la misma en todos los electrodos, pudiéndose comprobar que las masas de los distintos elementos liberados son proporcionales a sus respectivos equivalentes redox, obedeciendo asá la segunda ley.
la intensidad de corriente eléctrica. Si se hace pasar por una cuba electrolítica cierta intensidad durante diferentes lapsos de tiempo, las masas de un mismo elemento se muestran proporcionales a las respectivas cargas que han pasado por los electrodos. Por otra parte si se ponen en varias cubas en serie con distintos electrodos y disoluciones, es claro que la carga eléctrica que pasa es la misma en todos los electrodos, pudiéndose comprobar que las masas de los distintos elementos liberados son proporcionales a sus respectivos equivalentes redox, obedeciendo asá la segunda ley.
Un equivalente redox es la cantidad de sustancia que toma o cede un mol de electrones en una reacción redox.
Para liberar un equivalente en el electrodo de una célula electrolítica será preciso que pasen un mol de electrones, que portan una carga aproximada de 96 500 culombios (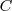 ), es decir,
), es decir, 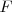 , la constante de Faraday o Faraday (
, la constante de Faraday o Faraday (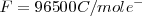 ;
; 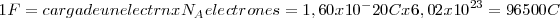 ; donde
; donde 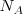 es el número de Avogadro ).
es el número de Avogadro ).
En la siguiente ecuación reúne en sí ambas leyes:
Donde:
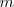 es la masa en gramos de elemento liberada en el electrodo;
es la masa en gramos de elemento liberada en el electrodo; 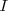 es la intensidad de la corriente en Amperios (A);
es la intensidad de la corriente en Amperios (A); 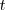 es el tiempo en segundos que ha pasado la corriente; y
es el tiempo en segundos que ha pasado la corriente; y 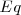 , el equivalente redox del elemento depositado:
, el equivalente redox del elemento depositado:
Ejemplo:
El paso de un mol de electrones en una cuba electrolítica de Dwon produce 1 mol (23.0 g ) de sodio en el cátodo:
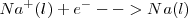
1 mol 1 mol 1 mol (23.0 g)
El paso de 1 mol de electrones en un proceso de Hall-Heroult produce 1/3 de mol (9.0 g) de aluminio, debido a que tres moles de electrones son requeridos para reducir un mol de 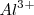 a aluminio metálico
a aluminio metálico 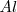 :
:
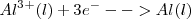
1/3 mol 1 mol 1/3 mol (9.0 g)
En general, la cantidad de producto formado en un electrodo se sigue directamente de la estequiometría de la reacción y de la masa molar del producto.
Tweet