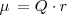Momento dipolar. El enlace de hidrógeno
De Wikillerato
Momento dipolar
El momento dipolar de dos cargas iguales y de signo opuesto se define como el producto de esta carga eléctrica (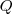 por la distancia
por la distancia  que las separa. Constituye una medida de la polaridad neta de la molécula.
que las separa. Constituye una medida de la polaridad neta de la molécula.
El momento bipolar es una magnitud dirigida, i.e. es una cantidad vectorial. Para el estudio de los momentos bipolares moleculares resulta adecuado introducir la unidad llamada debye. (D), llamada así en honor del físico-químico Peter J. W. Debye (1884-1966). Así los momentos bipolares son expresados en debyes (D), donde 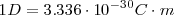 i.e. culombios por metro
i.e. culombios por metro
Por ejemplo si un protón y un electrón están separados por 100 pm (un poco menos que la longitud de un enlace covalente típico), entonces el momento bipolar sería 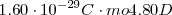
El átomo de cloro 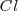 es más electronegativo que el del carbón
es más electronegativo que el del carbón 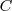 , y así por ejemplo en la molécula de clorometano (
, y así por ejemplo en la molécula de clorometano (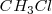 ) este atrae los electrones del enlace
) este atrae los electrones del enlace  hacia si mismo. El enlace
hacia si mismo. El enlace  se polariza por ello, así que el átomo de cloro es ligeramente más rico electrónicamente (representado con el símbolo
se polariza por ello, así que el átomo de cloro es ligeramente más rico electrónicamente (representado con el símbolo 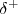 ) que el átomo de carbón que será ligeramente más pobre en electrones (
) que el átomo de carbón que será ligeramente más pobre en electrones (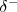 ). Debido a que el enlace polar
). Debido a que el enlace polar  en el clorometano tiene dos terminales polares (uno positivo y otro negativo) se dice por ello que es un enlace dipolar o dipolo y se representa frecuentemente usando una flecha con una cruz en uno de los terminales para indicar la dirección del desplazamiento electrónico. La punta de la flecha representa el terminal negativo del dipolo (
en el clorometano tiene dos terminales polares (uno positivo y otro negativo) se dice por ello que es un enlace dipolar o dipolo y se representa frecuentemente usando una flecha con una cruz en uno de los terminales para indicar la dirección del desplazamiento electrónico. La punta de la flecha representa el terminal negativo del dipolo (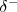 y el origen de la misma con una raya cruzandola por lo que parece un signo más) representa el terminal o polo positivo (
y el origen de la misma con una raya cruzandola por lo que parece un signo más) representa el terminal o polo positivo (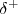 ).
).
Los momentos dipolares pueden ser medidos fácilmente de manera experimental y por ejemplo el valor de algunas sustancias relevantes son:





De la misma manera que los enlaces individuales en la molécula son frecuentemente polares, las moléculas como conjunto pueden ser también polares debido a la suma neta de las polaridades de los enlaces individuales y a la contribución de los pares solitarios de la molécula. El resultado es un dipolo molecular que puede ser visualizado de la siguiente manera: se asume que hay en la molécula un centro de masas de toda la carga positiva (núcleo) y un centro de masas de todas las cargas negativas (electrones). Si estos dos centros no coinciden, la molécula tiene una polaridad neta.
Enlace de hidrógeno
El enlace de hidrógeno es una interacción atractiva entre átomos de hidrógenos (de ahí su nombre) unidos a átomos muy electronegativos (O, N o F) y un par de electrones no compartidos en otro átomo electronegativo. El concepto fue introducido para la molécula del agua por los fisico-químicos Latimer y Rodesbush en 1920. Este tipo de enlace aparece en un número restringido de moléculas que poseen átomos de hidrógeno unidos a átomos muy electronegativos. El enlace entre el hidrógeno y el átomo electronegativo está muy polarizado debido a la diferencia de electronegatividad entre los átomos enlazados. Debido a que el hidrógeno no tiene más que el electrón que participa en el enlace, el desplazamiento de la pareja electrónica enlazante deja al protón casi desnudo de electrones, y con lo mismo con una alta densidad de carga eléctrica positiva. Debido a esta separación parcial de carga, el protón interaccionará electrostáticamente cuando tenga próxima una molécula con una pareja electrónica no enlazante formándose con ello una unión de tipo punte de hidrógeno.
Los átomos de hidrógeno se originan debido a que los enlaces 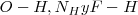 son altamente polares, con una carga parcial positiva en el hidrógeno y una carga parcial negativa en el átomo electronegativo. Además el hidrógeno no tinee electrones para proteger su núcleo, y tiene un pequeño tamaño así que puede aproximarse de manera cercana a otras moléculas. Como resultado, la atracción dipolo-dipolo entre el hidrógeno y par de electrones no compartidos en un átomo cercano es generalmente fuerte, dando origen al enlace de hidrógeno. Por ejemplo el agua es capaz de dar una vasta red tridimensional de enlaces de hidrógeno debido a que las moléculas de
son altamente polares, con una carga parcial positiva en el hidrógeno y una carga parcial negativa en el átomo electronegativo. Además el hidrógeno no tinee electrones para proteger su núcleo, y tiene un pequeño tamaño así que puede aproximarse de manera cercana a otras moléculas. Como resultado, la atracción dipolo-dipolo entre el hidrógeno y par de electrones no compartidos en un átomo cercano es generalmente fuerte, dando origen al enlace de hidrógeno. Por ejemplo el agua es capaz de dar una vasta red tridimensional de enlaces de hidrógeno debido a que las moléculas de 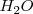 tienen dos hidrógenos y dos pares de electrones.
tienen dos hidrógenos y dos pares de electrones.
Como fuerza intermoleculares que son, lospuentes de hidrógeno no son verdaderos enlaces químicos pues la energía de los enlaces de hidrógeno es por término medio una veinte veces más baja, pero son más fuertes que las fuerzas de Van der Waals con energías de hasta 40 KJ/mol. Un aspecto importante de los puente de hidrógeno es que son direccionales, propiedad esta de suma importancia y que tendrá consecuencias transcedentales para las propiedades fisicoquímicas de las sustancias que los forman, en especial en el caso del agua y en la estructura y dinámica de importantes sistema supramoleculares biológicos. La fuerte influencia de los puentes de hidrógeno en la cohesión molecular queda reflejada en los puntos de fusión y ebullición anormalmente altos del agua, amoniaco y fluoruro de hidrógeno, si se los compara con los compuestos binarios de hidrógeno de los respectivos grupos de sistema periódico. Causan pues que el agua sea un líquido más bien que un gas a temperatura ordinaria y es la primera fuerza intermolecular que mantiene unidas las grandes biomoléculas en la forma necesaria para que tengan su papel esencial en la bioquímica. La famosa doble hélice de DNA tiene dos cadenas arrolladas una alrededor de la otra siendo mantenidas juntas por puentes de hidrógeno.
Tweet