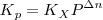Constante de equilibrio de las fracciones molares
De Wikillerato
(Página nueva: ==Constante de equilibrio de las fracciones molares== La constante <math> K_X </math> en función de las fracciones molares <math> X_i </math> se define por la siguiente relaci...) |
|||
| Línea 17: | Línea 17: | ||
Donde <math> X_i </math> es la fracción molar del gas <math> i </math> en la mezcla se cumple que: | Donde <math> X_i </math> es la fracción molar del gas <math> i </math> en la mezcla se cumple que: | ||
| - | <math>K_p= \frac{ [P_C]^{c} [P_D]^{d} }{[P_A]^{a} [P_B]^{b}} = \frac{ ( | + | <math>K_p= \frac{ [P_C]^{c} [P_D]^{d} }{[P_A]^{a} [P_B]^{b}} = \frac{ (X_C ∙ P)^c ∙ ( X_D∙ P)^d }{(X_A ∙ P)^{a} ∙ (X_B ∙ P)^b}}= \frac { [X_C]^{c} ∙ [X_D]^{d} }{[X_A]^{a} [X_B]^{b}} ∙ P^{(c+d)-(a+b)}} = K_X ∙ P^ {\Delta n} </math> |
Por tanto: | Por tanto: | ||
Revisión actual
Constante de equilibrio de las fracciones molares
La constante 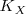 en función de las fracciones molares
en función de las fracciones molares 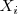 se define por la siguiente relación:
se define por la siguiente relación:
Donde la fracción molar 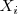 es la proporción, en moles, de una sustancia:
es la proporción, en moles, de una sustancia:
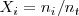 ; donde
; donde 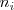 es el número de moles de
es el número de moles de  y
y 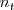 es número total de moles de la mezcla.
es número total de moles de la mezcla.
La suma de las fraciones molares de todos los gases de una mezcla es la unidad
Teniendo en cuenta que la relación entre la presión parcial de un gas, 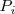 y la presión total de la mezcla de gases
y la presión total de la mezcla de gases 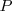 viene dada por la ley de Raoult:
viene dada por la ley de Raoult:
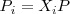
Donde 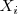 es la fracción molar del gas
es la fracción molar del gas  en la mezcla se cumple que:
en la mezcla se cumple que:
Por tanto:
Donde 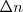 es la variación del número de moles (moles de productos menos moles de reactivos) en la ecuación química ajustada. Sólo se tiene en cuenta los moles de las sustancias gaseosas (pues la variación de la cocentración del resto de sustanias será desprecible).
es la variación del número de moles (moles de productos menos moles de reactivos) en la ecuación química ajustada. Sólo se tiene en cuenta los moles de las sustancias gaseosas (pues la variación de la cocentración del resto de sustanias será desprecible).
Si no existe varción en el número de moles entonces 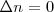 , lo que implica
, lo que implica
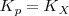
La constante 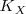 depende de la temperatura y de la presión total del equilibrio. Las constantes
depende de la temperatura y de la presión total del equilibrio. Las constantes 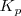 y
y 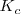 , dependen solo de la temperatura.
, dependen solo de la temperatura.


![K_X=\frac{ [X_C]^{c} [X_d]^{D}}{[X_A]^{a} [X]^{b}} K_X=\frac{ [X_C]^{c} [X_d]^{D}}{[X_A]^{a} [X]^{b}}](/images/math/math-fcf1572913ea101d5172aa15f256ebe2.png)
![K_p= \frac{ [P_C]^{c} [P_D]^{d} }{[P_A]^{a} [P_B]^{b}} = \frac{ (X_C � P)^c � ( X_D� P)^d }{(X_A � P)^{a} � (X_B � P)^b}}= \frac { [X_C]^{c} � [X_D]^{d} }{[X_A]^{a} [X_B]^{b}} � P^{(c+d)-(a+b)}} = K_X � P^ {\Delta n} K_p= \frac{ [P_C]^{c} [P_D]^{d} }{[P_A]^{a} [P_B]^{b}} = \frac{ (X_C � P)^c � ( X_D� P)^d }{(X_A � P)^{a} � (X_B � P)^b}}= \frac { [X_C]^{c} � [X_D]^{d} }{[X_A]^{a} [X_B]^{b}} � P^{(c+d)-(a+b)}} = K_X � P^ {\Delta n}](/images/math/math-1102604c30a7bc98c09f4f1f7eb9fb66.png)